近年來,腫瘤免疫治療領域風起云涌、日新月異,好消息不斷傳來,其中程序性死亡受體-1(PD-1)抑制劑更是一枝獨秀、獨領風騷。進口PD-1抑制劑早已上市,由中國創新藥企自主研發的PD-1抑制劑也已經陸續面世,其中2019年12月國家藥品監督管理局(NMPA)批準上市的本土創新PD-1抑制劑百澤安(替雷利珠單抗注射液,BGB-317)便是其中濃墨重彩的一筆。那么,在市場上眾多PD-1抑制劑中,百澤安有何獨特的魅力呢?隨小編來一探究竟。
認識百澤安
百澤安是由中國創新生物制藥企業百濟神州自主研發的一款PD-1抑制劑,于2019年12月經國家藥品監督管理局(NMPA)批準上市,現已獲批用于治療至少經過二線系統化療的復發或難治性經典型霍奇金淋巴瘤(r/r cHL),和用于治療PD-L1高表達的含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌(UC)。
此外,多種適應證上市申請已獲得NMPA受理,包括聯合化療用于治療一線晚期鱗狀非小細胞肺癌與一線晚期非鱗狀非小細胞肺癌,以及用于治療既往接受過治療的不可切除肝細胞癌(HCC)。同時,百澤安正在肺癌、食管鱗癌、肝癌、胃癌、鼻咽癌、婦科腫瘤及高位衛星不穩定(MSI-H)或錯配修復缺陷性(dMMR)實體瘤在內多個瘤種開展16項潛在注冊性臨床試驗,為造福更多患者而努力。
生而不同 結構優化
1.認識PD -1 抑制劑
PD-1抑制劑作為免疫治療的“寵兒”,是怎樣發揮抗腫瘤作用的呢,我們來看一看。
T細胞表面有PD-1受體,是一種重要的免疫抑制分子,一旦打開“開關”,便可抑制T細胞活性。PD-1的配體PD-L1是打開“開關”的重要因素,狡猾的腫瘤細胞表面則含有PD-L1,可幫助腫瘤細胞“躲避”免疫細胞的追殺。而以PD-1抑制劑為代表的免疫檢查點抑制劑,其作用就是阻止T細胞表面的PD-1受體和腫瘤表明的PD-L1配體的結合,使腫瘤細胞逃無可逃。
2.結構 優化
百澤安在傳統PD-1抗體的基礎上,進一步優化了分子結構,使其抗腫瘤作用更明顯。
l Fc段獨特改造
PD-1抗體通常選用IgG4抗體,但IgG4抗體仍保留部分ADCP效應(抗體依賴的細胞介導的吞噬作用),會導致巨噬細胞吞噬T細胞,進而影響治療效果。百澤安是目前唯一一款對Fc段進行獨特結構改造的PD-1抗體,去除了自身與巨噬細胞表面FCyR結合的能力,從而消除了ADCP效應,避免了因T細胞數量減少而影響抗腫瘤作用。
l Fab段更大程度持久阻斷
相較于其他PD-1抗體,百澤安特有的抗原結合表位,使其Fab段與PD-1的結合面與PD-1/L1的結合面大范圍重疊,可更大程度阻斷PD-1與PD-L1的結合。
此外,百澤安還具有優異的結合動力學表現,Fab段與PD-1的親和力高于同類抗體,從PD-1上解離的速率慢,與PD-1的結合更持久,發揮持久阻斷作用。
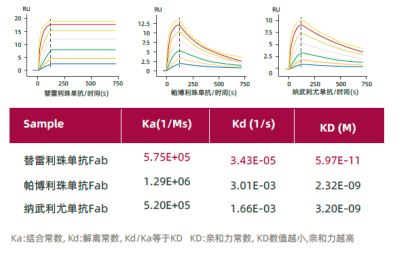
圖 1 不同PD-1 藥物的 親和力 及 解離速率 情況對比
l 半衰期 長
有研究表明,抗體半衰期越長,抗腫瘤活性越強。與其他PD-1抗體相比,百澤安的終末半衰期約為26天,高于其他同類藥物,預示了其良好的抗腫瘤活性。
l 抗腫瘤 活性強
百澤安的IC50和EC50均達到了同類藥物的最低范圍。IC50(半數抑制濃度)即一種藥物能將細胞生長、病毒復制等抑制50%所需的濃度,EC50(半數效應濃度)即引起受試對象50%個體產生一種特定效應的藥物劑量,IC50和EC50值越低,代表抗腫瘤活性越好。
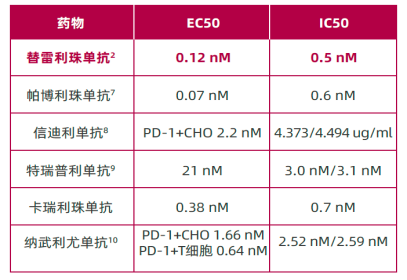
圖 2 不同PD-1藥物 的 IC50、EC50情況 對比
生而不凡 臨床數據亮眼
l 復發或難治性經典型霍奇金淋巴瘤(r/r cHL)
RATIONALE 203研究為一項評價百澤安單藥治療中國r/r cHL患者的單臂、多中心、II期研究,共納入70例患者,所有患者均接受替雷利珠單抗200mg,靜脈給藥,每3周一次,直至出現疾病進展、不可接受的毒性反應或研究終止。主要終點為獨立審查委員會根據Lugano 2014分類評估的總緩解率(ORR),該研究結果于2019年9月在權威學術期刊Leukemia雜志公開發表。
研究結果顯示,中位隨訪時間9.8個月,61例患者(87.1%)獲得客觀緩解,其中44例患者(62.9%)獲得完全緩解(CR),與其他PD-1抗體治療r/r cHL相比(非頭對頭比較),完全緩解(CR)率更高,獲益更明顯。
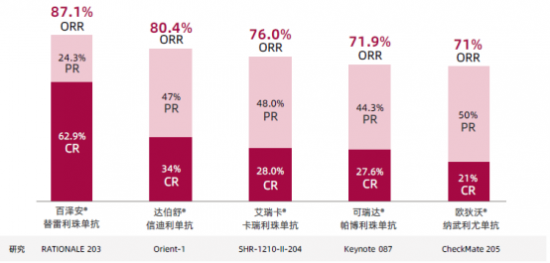
圖 3 各PD-1抗體單藥治療r/r cHL的II期研究的緩解率數據(非頭對頭比較)
百澤安治療r/r cHL安全性良好,不良反應多為一、二級,免疫相關的不良反應發生率為38.6%,無患者發生嚴重超敏/過敏反應,未發生因不良事件而導致的死亡。
l 鱗狀非小細胞肺癌(NSCLC)
RATIONALE 307研究是一項III期、多中心、隨機、開放研究,旨在評價百澤安聯合紫杉醇/白蛋白紫杉醇+卡鉑一線治療局部晚期或轉移性鱗狀NSCLC的有效性和安全性。這是中國首個、全球第二個成功且中國入組人數最多的肺鱗癌一線免疫聯合治療的Ⅲ期臨床研究。
2020 ASCO年會公布該研究中位隨訪8.6個月的中期分析結果,研究顯示,替雷利珠單抗+白蛋白紫杉醇+卡鉑組的中位無進展生存期(mPFS)達7.6個月,疾病進展風險降低52%;替雷利珠單抗+紫杉醇+卡鉑組的mPFS達7.6個月,疾病進展風險降低48%;化療對照組mPFS為5.5個月。
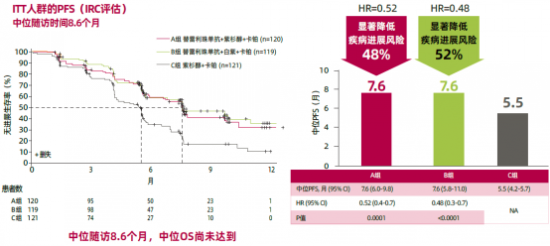
圖 4 RATIONALE 307研究PFS結果
替雷利珠單抗+白蛋白紫杉醇+卡鉑組的ORR達74.8%,替雷利珠單抗+紫杉醇+卡鉑組的ORR達72.5%,化療對照組為49.6%。替雷利珠單抗+白蛋白紫杉醇+卡鉑組的中位持續緩解時間(mDoR)達8.6個月,替雷利珠單抗+紫杉醇+卡鉑組的mDoR達8.2個月,化療對照組為4.2個月。
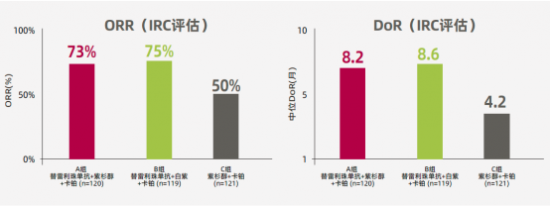
圖 5 RATIONALE 307研究 ORR 、 DoR 結果
百澤安聯合化療一線治療晚期肺鱗癌患者安全性、耐受性良好,報告的治療相關不良事件與已知的雙藥化療的安全性譜一致;在雙藥化療基礎上聯合百澤安并未出現新的安全性信號。
l 肝癌(HCC)
RATIONALE 001研究是一項百澤安單藥治療晚期實體瘤的IA/IB期全球研究,共納入50例晚期肝細胞癌患者。其中,肝炎病毒感染患者比例高達92%。研究結果顯示,總體人群疾病控制率(DCR)達51%,其中二線人群ORR達到18.8%。
百澤安在晚期經過治療的HCC中耐受性良好,且AE譜與其他腫瘤類型類似,二線及二線之后治療晚期肝癌患者常見不良反應中≥3級的發生率為10%(常見不良反應指所有級別的發生率≥10%的不良反應)。
l 鼻咽癌(NPC)
RATIONALE 102研究是一項多中心、開放標簽的I/II期臨床研究,2019年ASCO、CSCO學術年會和今年Journal for Immuno Therapy of Cancer雜志(IF:9.9)更新了研究結果。研究顯示,百澤安單藥后線治療NPC,客觀緩解率(ORR)為43%,為目前已報道PD-1抑制劑單藥治療NPC的最高ORR數據,疾病控制率(DCR)高達86%,中位無進展生存期(PFS)為10.4個月,整體中位總生存期未達到。同時,百澤安單藥治療NPC,大部分AE為輕中度,安全性良好。
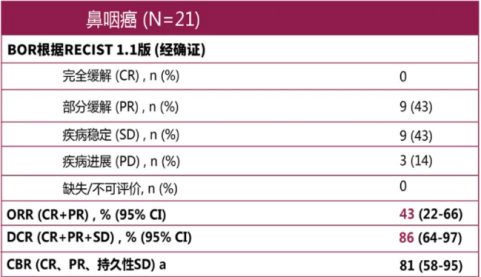
圖 6 百澤安 單藥治療晚期 NPC的緩解 情況
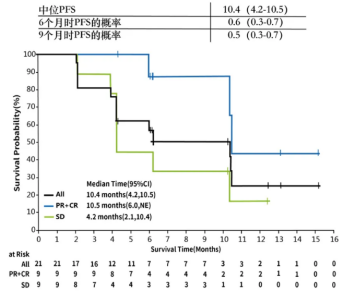
圖7 百澤安 單藥治療晚期 NPC的PFS數據
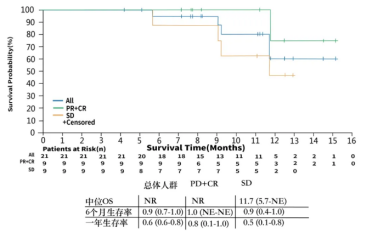
圖8 百澤安 單藥治療晚期 NPC的OS數據
百澤安作為中國本土創新生物制藥企業百濟神州自主研發的一款PD-1抑制劑,不僅有亮眼的研究數據,還有嚴格的質量管控以及惠民的援助政策。自進入臨床研究階段起,百澤安不斷帶來驚喜,其卓越的療效也與其創新的結構優化密不可分。未來,將會有更多適應證獲批,為腫瘤治療的發展帶來新氣象,讓我們拭目以待!
本網站所有信息僅供參考,不做個別診斷、用藥和使用的根據。本網站致力于提供正確、完整的健康內容的真實性,我們不對其科學性、嚴肅性等作任何形式的保證。如其他媒體、網絡或個人從本網下載使用須自負版權等法律責任。
本網站所有信息僅供參考,不做個別診斷、用藥和使用的根據。本網站致力于提供正確、完整的健康資訊,但不保證信息的正確性和完整性,且不對因信息的不正確或遺漏導致的任何損失或損害承擔責任。本站所提供的任何醫藥資訊,僅供參考,不能替代醫生和其他醫務人員的建議,如自行使用本網資料發生偏差,本站概不負責,亦不負任何法律責任。
